Pur ammettendo specifiche differenza da caso a caso, una caratteristica comune alla maggior parte dei tumori è data dai bassi livelli di ossigeno. Come dimostrato da numerose indagini, in condizioni di ipossia i tumori hanno generalmente un comportamento più aggressivo e le cellule tumorali subiscono frequenti mutazioni genetiche, sviluppando in tal modo una straordinaria capacità di diffondersi e, quindi, di portare a metastasi.
L’ipossia (carenza di ossigeno) nella radio e chemioterapia
L’ipossia a livello del tessuto tumorale non solo porta ad una maggiore aggressività del tumore, ma causa anche una bassa risposta alla chemio e radioterapia.
In particolare, l’efficacia dei farmaci antitumorali è risultata essere ostacolata sia dai bassi livelli di ossigeno che dalle condizioni di acidosi del tessuto corporeo dovute alla glicolisi anaerobica, condiszione anch’essa legata alla carenza di ossigeno. Poiché alcuni farmaci chemioterapici richiedono ossigeno per generare i radicali liberi che uccidono le cellule tumorali, gli stessi farmaci si sono dimostrati essere inefficaci (o meno efficaci) nel caso di un cancro particolarmente ipossico.
Studio: “Effects of hypoxia on human cancer cell line chemosensitivity“
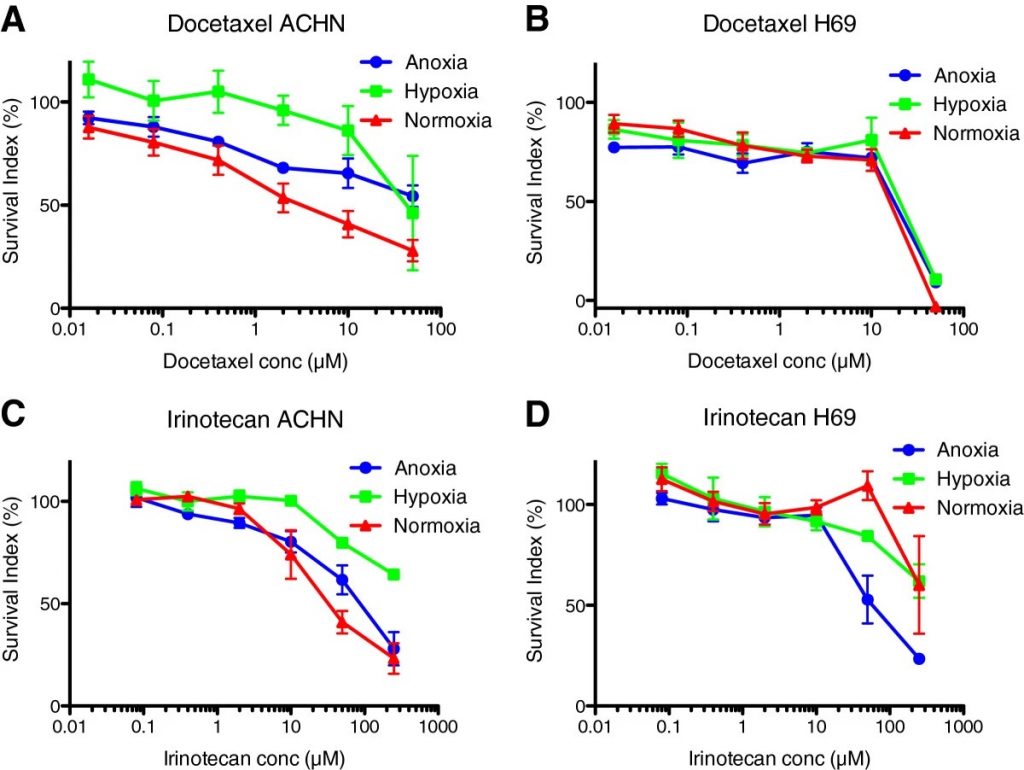
Per renderne la consultazione più semplice, riportiamo di seguito la traduzione dell’absctract dello studio “Effects of hypoxia on human cancer cell line chemosensitivity” condotto dai ricercatori Sara Strese, Mårten Fryknäs, Rolf Larsson e Joachim Gullbo integralmente consultabile cliccando qui.
Metodo
Sono stati testati un panel di 19 farmaci disponibili in commercio: 5-fluorouracile, acriflavina, bortezomib, cisplatino, digitossina, digossina, docetaxel, doxorubicina, etoposide, gemcitabina, irinotecan, melfalan, mitomicina c, rapamicina, sorafenib, talidomide, toscritina e tiracanpazamina, per l’attività citotossica sulle linee cellulari tumorali A2780 (ovarico), ACHN (renale), MCF-7 (seno), H69 (SCLC) e U-937 (linfoma). Parti uguali e parallele delle cellule sono state coltivate a diverse pressioni di ossigeno e dopo 72 ore di esposizione al farmaco è stata ne è stata misurata la vitalità (citotossicità in microcoltura fluorimetrica FMCA).
Resistenza mediata dall’ipossia alla radio e chemioterapia
Le cellule ipossiche, cioè in carenza di ossigeno, possono essere resistenti sia alla radioterapia che alla chemioterapia convenzionale.
Gli studi dimostrano l’impatto negativo dell’ipossia sull’efficacia della radioterapia nel trattamento tumorale e, in particolare, nel caso di carcinoma mammario, carcinoma della testa e del collo e carcinoma della cervice uterina. Esistono diverse teorie non escluse per spiegare il fatto che anche la chemioterapia convenzionale abbia un effetto minore sulle cellule tumorali ipossiche. Il pattern vascolare anarchico caratteristico di molti tumori include cambiamenti di calibro, anse e triforcazioni. Unitamente alla distanza tra cellula e vaso sanguigno, ciò diminuisce sia l’esposizione del farmaco antitumorale che la proliferazione cellulare. Poiché l’effetto citotossico è maggiore nelle cellule in rapida divisione, le cellule tumorali a lenta proliferazione lontane dai vasi sanguigni risultano essere meno sensibili alla chemioterapia. Da momento che l’ipossia coinvolge anche le cellule con bassa espressione di p53, di conseguenza l’apoptosi indotta da p53 risulta conseguentemente ridotta nelle cellule ipossiche. Inoltre, in un ambiente normossico (cioè con normali livelli di ossigeno), le lesioni al DNA causate da alcuni farmaci antitumorali sono più permanenti, mentre in un ambiente ipossico si verificano livelli più elevati di ripristino e guarigione.
Leggi anche – Ipossia tumorale

